জৈব যৌগগুলির প্রাথমিক শ্রেণিবিভাগ (Elementary Classification of Organic Compounds) :
কার্যকরী মূলকের ওপর ভিত্তি করে জৈব যৌগগুলিকে বিভিন্ন শ্রেণিতে ভাগ করা যায় । যথা :-
[1] হাইড্রোকার্বন
[2] অ্যালকোহল
[3] অ্যালডিহাইড
[4] কিটোন
[5] কার্বক্সিলিক অ্যাসিড যৌগ
নীচে জৈব যৌগের কয়েকটি শ্রেণি এবং প্রতিটি শ্রেণির প্রথম তিনটি সদস্যের নাম ও গঠন দেওয়া হল :
[1] হাইড্রোকার্বন (Hydrocarbons)
যেসব জৈব যৌগ শুধু কার্বন ও হাইড্রোজেন পরমাণু দিয়ে গঠিত তাদের হাইড্রোকার্বন বলে । যথা : মিথেন (CH4), ইথেন (C2H6), ইথিলিন (C2H4), অ্যাসিটিলিন (C2H2) ইত্যাদি । যেসব জৈব যৌগের গঠনে প্রান্তের কার্বন পরমাণুগুলি মুক্ত থাকে তাদের মুক্ত শৃঙ্খল জৈব যৌগ বলে । যেমন, প্রপেন একটি মুক্ত শৃঙ্খল জৈব যৌগ : CH3CH2CH3 প্রপেন (মুক্ত শৃঙ্খল যৌগ) এখানে শুধু মুক্ত শৃঙ্খল জৈব যৌগ আলোচনা করা হল ।
মুক্ত শৃঙ্খল হাইড্রোকার্বনগুলিকে দুটি ভাগে ভাগ করা যায়: [i] সম্পৃক্ত হাইড্রোকার্বন (Saturated Hydrocarbons) এবং [ii] অসম্পৃক্ত হাইড্রোকার্বন (Unsaturated Hydrocarbons) ।
[i] সম্পৃক্ত হাইড্রোকার্বন (Saturated Hydrocarbons) :- শুধু কার্বন বা হাইড্রোজেন দিয়ে গঠিত মুক্ত শৃঙ্খল জৈব যৌগ যাদের গঠনে শুধু কার্বন-কার্বন এক-বন্ধন (C - C) এবং / অথবা কার্বন-হাইড্রোজেন এক বন্ধন (C - H) থাকে তাদের মুক্ত শৃঙ্খল সম্পৃক্ত হাইড্রোকার্বন বা প্যারাফিন বলে । এদের নামের শেষে 'এন্' (ane) কথাটি যুক্ত থাকে, এদের অ্যালকেন (Alkane) বলে । এদের সাধারণ সংকেত CnH2n+2 ( যেখানে n হল কার্বন পরমাণুর সংখ্যা ) । যথা : মিথেন (CH4), ইথেন (C2H6), প্রোপেন (C3H8) ইত্যাদি ।
অ্যালকেনের প্রথম তিনটি সদস্যের গঠন ও নাম—
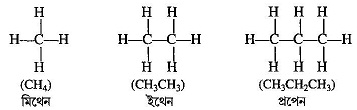
[ii] অসম্পৃক্ত হাইড্রোকার্বন (Unsaturated Hydrocarbons):- যে সব হাইড্রোকার্বনের গঠনে এক বা একাধিক কার্বন-কার্বন দ্বি-বন্ধনী ( > C = C < ) বা ত্রি-বন্ধনী ( — C ≡ C — ) থাকে, তাদের অসম্পৃক্ত হাইড্রোকার্বন বলে । অসম্পৃক্ত হাইড্রোকার্বন দু-ধরনের হয় : যথা- [a] অ্যালকিন এবং [b] অ্যালকাইন ।
[a] অ্যালকিন (Alkene) : যে সব হাইড্রোকার্বনের গঠনে এক বা একাধিক কার্বন-কার্বন দ্বি-বন্ধনী ( > C = C < ) থাকে, তাদের অ্যালকিন (Alkene) বলে । এদের নামের শেষে 'ইন' (ene) কথাটি যুক্ত থাকে । এদের রাসায়নিক সংকেত হল CnH2n । IUPAC অনুসারে এদের কার্যকরী মূলক ( > C = C < ) । যথা: ইথিলিন বা ইথিন (C2H4), প্রোপিলিন বা প্রোপিন (C3H6), বিউটিলিন (C4H8) ইত্যাদি । অ্যালকিন একটি (> C = C <) শ্রেণি যুক্ত মুক্ত শৃঙ্খল হাইড্রোকার্বন ।
অ্যালকিনের প্রথম তিনটি সদস্যের গঠন ও নাম—
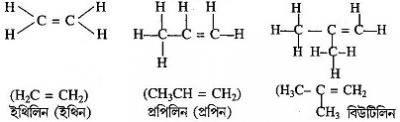
[b] অ্যালকাইন (Alkyne) : যে সব হাইড্রোকার্বনের গঠনে এক বা একাধিক কার্বন-কার্বন ত্রি-বন্ধনী ( — C ≡ C — ) থাকে, তাদের অ্যালকাইন বলে । এদের নামের শেষে 'আইন' (yne) কথাটি যুক্ত থাকে । এদের রাসায়নিক সংকেত হল CnH2n-2 । IUPAC অনুসারে এদের কার্যকরী মূলক ( — C ≡ C — ) । অ্যালকাইন একটি ( — C ≡ C — ) শ্রেণি যুক্ত মুক্ত শৃঙ্খল হাইড্রোকার্বন । যথা: অ্যাসিটিলিন ( HC ≡ CH ), মিথাইল অ্যাসিটিলিন ( CH3C ≡ CH ), ডাইমিথাইল অ্যাসিটিলিন ( H3C - C ≡ C - CH3 ) ইত্যাদি ।
অ্যালকাইনের প্রথম তিনটি সদস্যের গঠন ও নাম—
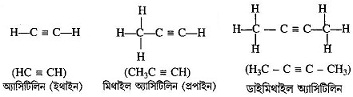
[2] অ্যালকোহল (Alcohols) :
অ্যালকেনের এক বা একাধিক হাইড্রোজেন পরমাণু হাইড্রক্সিল গ্রুপ (—OH) দ্বারা প্রতিস্থাপিত হয়ে যে যৌগ উৎপন্ন করে, তাদের অ্যালকোহল শ্রেণির যৌগ বলে । অর্থাৎ R-H ( অ্যালকেন ) থেকে R-OH ( অ্যালকোহল ) । যেসব অ্যালকোহল যৌগে (-CH2OH) গ্রুপ থাকে, তাদের প্রাইমারী অ্যালকোহল বলে । IUPAC অনুসারে অ্যালকোহল শ্রেণির যৌগের কার্যকরী মূলক —OH । এদের নামের শেষে 'অনল' কথাটি যুক্ত থাকে । অ্যালকোহল হল কার্যকরী মূলক -OH যুক্ত মুক্ত শৃঙ্খল যৌগ । এই শ্রেণির সাধারণ সংকেত হল CnH2n+1, যেখানে n= কার্বন পরমাণুর সংখ্যা । যেমন: মিথাইল অ্যালকোহল বা মিথানল (CH3OH), ইথাইল অ্যালকোহল বা ইথানল (CH3CH2OH), প্রোপাইল অ্যালকোহল বা প্রোপানল (CH3CH2CH2OH) ।
উদাহরণ:
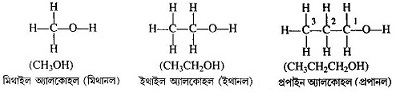
[3] অ্যালডিহাইড (Aldehydes) :
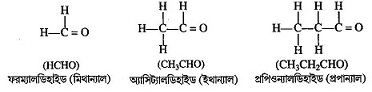
অ্যালকেনের একটি হাইড্রোজেন পরমাণু (—CHO) গ্রুপ দ্বারা প্রতিস্থাপিত হলে, তাদের অ্যালডিহাইড শ্রেণির যৌগ বলে । IUPAC অনুসারে অ্যালডিহাইড শ্রেণির যৌগের কার্যকরী মূলক -CHO । এদের নামের শেষে 'অ্যাল' কথাটি যুক্ত থাকে । অ্যালডিহাইডের সাধারণ সংকেত R—CHO, যেখান R হল অ্যালকিল মূলক, কেবলমাত্র প্রথম যৌগ ফরম্যালডিহাইড ( H—CHO ) এর ক্ষেত্রে R = H । যেমন : ফরম্যালডিহাইড বা মিথান্যাল (HCHO), অ্যাসিট্যালডিহাইড বা ইথান্যাল (CH3CHO), প্রোপিয়োন্যালহাইড বা প্রোপান্যাল (CH3CH2CHO), ইত্যাদি ।
উদাহরণ:
[4] কিটোন (Ketones):
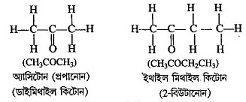
যে সব জৈব যৌগে কিটোনিক গ্রুপ থাকে, তাদের কিটোন শ্রেণির যৌগ বলে । এই শ্রেণির যৌগের কার্যকরী মূলক ( > C = O ) , কার্বনের দুটি যোজ্যতাই কার্বন পরমাণু দ্বারা তৃপ্ত । এই যৌগে কার্যকরী মূলকের সঙ্গে দুটি অ্যালকিল মূলক ( ভিন্ন বা অভিন্ন ) যুক্ত থাকে ।
উদাহরণ:
[5] কার্বক্সিলিক অ্যাসিড যৌগ (Carboxylic Acid):
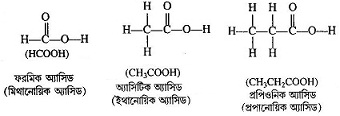
অ্যালকেনের হাইড্রোজেন পরমাণু (—COOH) গ্রুপ দ্বারা প্রতিস্থাপিত হয়ে যে যৌগ উৎপন্ন করে, তাদের কার্বক্সিলিক অ্যাসিড শ্রেণির যৌগ বলে । এদের ফ্যাটি অ্যাসিডও বলা হয় । এই শ্রেণির যৌগের কার্যকরী মূলক -COOH । কার্বক্সিলিক অ্যাসিডের সাধারণ সংকেত RCOOH, যেখানে R অ্যালকিল মূলক ; কেবলমাত্র প্রথম যৌগ ফরমিক অ্যাসিডের ক্ষেত্রে R = H ।
উদাহরণ:
*****
- 21390 views






