সালফিউরিক অ্যাসিডের ধর্ম (Properties of Sulphuric acid) :
ভৌত ধর্ম :-
[i] বিশুদ্ধ সালফিউরিক অ্যাসিড বর্ণহীন, গন্ধহীন, তেলের মতো ভারী তরল পদার্থ । সেজন্য একে অয়েল অফ ভিট্রিয়ল বলে ।
[ii] সালফিউরিক অ্যাসিডের স্বাদ অম্ল ও আপেক্ষিক গুরুত্ব 1.84 ;
[iii] সালফিউরিক অ্যাসিডের স্ফুটনাঙ্ক 338°C ও হিমাঙ্ক 10.4°C ।
[iv] জলের সঙ্গে যেকোনো অনুপাতে মেশে ।
জলীয় দ্রবণ প্রস্তুতের সময় গাঢ় সালফিউরিক অ্যাসিডের মধ্যে কখনো জল ঢালা উচিত নয়, কারণ— জল, গাঢ় সালফিউরিক অ্যাসিডের সংস্পর্শে এলে প্রচুর তাপ উৎপন্ন হয় । এজন্য গাঢ় সালফিউরিক অ্যাসিডের মধ্যে জল ঢাললে প্রচন্ড তাপে জল হঠাৎ বাষ্পে পরিণত হয়, ফলে বিস্ফোরকের মতো পাত্র থেকে উৎক্ষিপ্ত হয় । এজন্য সালফিউরিক অ্যাসিডের জলীয় দ্রবণ তৈরি করতে হলে কখনো অ্যাসিডের মধ্যে জল ঢালা উচিৎ নয় । জলের মধ্যে ধীরে ধীরে অল্প অল্প করে সালফিউরিক অ্যাসিড যোগ করে নাড়তে হয় ।
রাসায়নিক ধর্ম :-
[i] জলের প্রতি আসক্তি:- জলের প্রতি গাঢ় সালফিউরিক অ্যাসিডের তীব্র আসক্তি আছে, তাই গাঢ় H2SO4 একটি তীব্র নিরুদক । চিনি, কাগজ, স্টার্চ জাতীয় পদার্থের জলীয় উপাদান শোষণ করে পদার্থগুলিকে কালো কার্বনে পরিণত করে ।
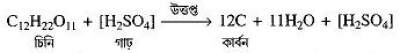
ফরমিক অ্যাসিড থেকে 1 অণু H2O শোষণ করে কার্বন মনোঅক্সাইডে পরিণত করে ।
HCOOH + H2SO4 = CO + [H2O + H2SO4]
এই ধর্মের জন্য, আর্দ্র গ্যাস যার সঙ্গে গাঢ় H2SO4 -এর বিক্রিয়া হয় না, সেগুলি (O2, H2, Cl2, N2, CO2 প্রভৃতি) শুষ্ক করতে গাঢ় H2SO4 ব্যবহৃত হয় ।
[ii] তাপের ক্রিয়া :- লোহিত-তপ্ত ঝামা পাথরের ওপর ফোঁটা ফোঁটা গাঢ় H2SO4 ফেললে বিয়োজিত হয়ে জল, সালফার ডাই অক্সাইড এবং অক্সিজেন উৎপন্ন করে । এই অক্সিজেন অন্য পদার্থকে জারিত করে ।
2H2SO4 = 2H2O + 2SO2 + O2
সালফিউরিক অ্যাসিডের সংস্পর্শে মার্বেল পাথরের তৈরি ইমারত ক্ষতিগ্রস্ত হতে পারে । কারণ— সালফিউরিক অ্যাসিডের সঙ্গে মার্বেল পাথর (CaCO3) -এর রাসায়নিক বিক্রিয়া হয়, ফলে মার্বেল পাথরের তৈরি ইমারত ক্ষতিগ্রস্ত হয় । রাসায়নিক বিক্রিয়াটি হল—
CaCO3 + H2SO4 = CaSO4 + CO2↑ + H2O
[iii] জারণ ক্ষমতা :- উষ্ণ এবং গাঢ় সালফিউরিক অ্যাসিড (H2SO4) বিয়োজিত হয়ে জায়মান অক্সিজেন দেয় । এজন্য গাঢ় H2SO4 -এর জারণ ক্ষমতা দেখা যায় ।
H2SO4 = H2O + SO2 + O↑
গাঢ় H2SO4 কার্বনকে জারিত করে কার্বন ডাইঅক্সাইডে পরিণত করে ।
2H2SO4 + C = CO2 + 2SO2 + 2H2O
[iv] ধাতুর সঙ্গে বিক্রিয়া :- ঠান্ডা ও লঘু সালফিউরিক অ্যাসিডের (H2SO4) সঙ্গে Fe, Mg, Al, Zn প্রভৃতি ধাতুর বিক্রিয়ায় সালফেট লবণ সৃষ্টি হয় এবং H2 গ্যাস বেরোয় ।
Fe + H2SO4 = FeSO4 + H2↑ ; Mg + H2SO4 = MgSO4 + H2↑
2Al + 3H2SO4 = Al2 (SO4)3 + 3H2↑ ; Zn + H2SO4 = ZnSO4 + H2↑
ঘন ও উত্তপ্ত H2SO4 -এর সঙ্গে Cu -এর বিক্রিয়ায় সালফেট লবণ ও SO2 গ্যাস উৎপন্ন হয় । ঠান্ডা অ্যাসিডের সঙ্গে কোনো বিক্রিয়া হয় না ।
Cu + 2H2SO4 (ঘন ও গরম) = CuSO4 + SO2↑ + 2H2O
H2SO4 শনাক্ত করণ :- গাঢ় বা লঘু H2SO4 কিংবা সালফেট লবণের জলীয় দ্রবণের সঙ্গে বেরিয়াম ক্লোরাইড অথবা বেরিয়াম নাইট্রেট দ্রবণ যোগ করলে বেরিয়াম সালফেটের সাদা অধঃক্ষেপ পড়ে । এই অধঃক্ষেপ HCl বা HNO3 -তে অদ্রাব্য । এই বিক্রিয়া দ্বারা H2SO4 এবং সালফেট লবণ শনাক্ত করা যায় ।
H2SO4 + BaCl2 = BaSO4↓ + 2HCl
(NH4)2SO4 + Ba(NO3)2 = BaSO4↑ + 2NH4NO3
*****
- 14809 views






