অ্যাম্মিটার এবং ভোল্টমিটারের ব্যবহার (Use of Ammeter and Voltameter) :
কোনো বর্তনীতে তড়িৎপ্রবাহ হচ্ছে কিনা, কিংবা হলে তার মান নির্ণয় করতে যে যন্ত্র ব্যবহার করা হয়, সেই যন্ত্রকে গ্যালভানোমিটার (Galvanometre) বলে । ইটালির বিজ্ঞানী লুইগি গ্যালভানির নামে এই যন্ত্রের নামকরণ হয়েছে । তড়িৎপ্রবাহের ওপর চুম্বকের ক্রিয়া এই মূল নীতির ওপর নির্ভর করে যে সব গ্যালভানোমিটার উদ্ভাবিত হয়েছে তাদের বলা হয় চলকুণ্ডলী গ্যালভানোমিটার । অ্যাম্মিটার এবং ভোল্টমিটার চলকুণ্ডলী গ্যালভানোমিটারের কার্যনীতি অনুযায়ী কাজ করে ।
অ্যাম্মিটারের সাহায্যে কোনো বর্তনীর তড়িৎপ্রবাহের মান নির্ণয় করা হয় । ভোল্টমিটারের সাহায্যে কোনো বর্তনীর দুটি বিন্দুর মধ্যে বিভব-প্রভেদ মাপা হয় ।
ব্যবহারের প্রয়োজনীয়তা অনুযায়ী গ্যালভানোমিটার কুণ্ডলীর সমান্তরাল সমবায়ে নিম্নমানের রোধ (সান্ট) জুড়ে যন্ত্রটিকে অ্যাম্মিটার হিসাবে এবং কুণ্ডলীর সঙ্গে শ্রেণি সমবায়ে উচ্চমানের রোধ জুড়ে যন্ত্রটিকে ভোল্টমিটার হিসাবে ব্যবহার করা হয় । অ্যাম্মিটারের স্কেল অ্যাম্পিয়ারে এবং ভোল্টমিটারের স্কেল ভোল্টে অংশাঙ্কিত (calibrated) করা থাকে ।
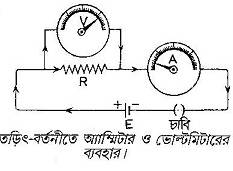
উপরের চিত্রানুযায়ী বর্তনীর তড়িৎপ্রবাহ পরিমাপ করতে অ্যাম্মিটার A -কে বর্তনীতে শ্রেণি সমবায়ে যুক্ত করতে হয় যেন বর্তনীর মূল প্রবাহ সরাসরি যন্ত্রের ভিতর দিয়ে যায় । বর্তনীর কোনো অংশের বিভব-প্রভেদ পরিমাপ করতে, যেমন R রোধের দু'প্রান্তের বিভব-প্রভেদ মাপতে হলে, ভোল্টমিটার V -কে R -এর সমান্তরালে এর দু'প্রান্তে যুক্ত করতে হয়, যেন মূল প্রবাহের এক অংশ যন্ত্রের ভিতর দিয়ে প্রবাহিত হয় ।
অ্যাম্মিটারের পরিমাপের পাল্লা (range) বৃদ্ধি করতে ওই যন্ত্রের কুণ্ডলীর সঙ্গে সমান্তরালে যুক্ত সান্ট রোধের মান হ্রাস করতে হয় । ভোল্টমিটারের পরিমাপের পাল্লা বৃদ্ধি করতে যন্ত্রের কুণ্ডলীর সঙ্গে শ্রেণি সমবায়ে যুক্ত রোধের মান বৃদ্ধি করতে হয় ।
*****
- 6343 views






